Getty Images
Key Takeaways
- Pārtikas un zāļu pārvalde (FDA) prasīs vakcīnu ražotājiem divu mēnešu drošības datus, pirms tā apstiprinās vakcīnu COVID-19 lietošanai plašākai sabiedrībai.
- FDA uzskata, ka divu mēnešu periods ļaus pietiekami daudz laika iespējamās vakcīnas iespējamām blakusparādībām vai nelabvēlīgiem rezultātiem.
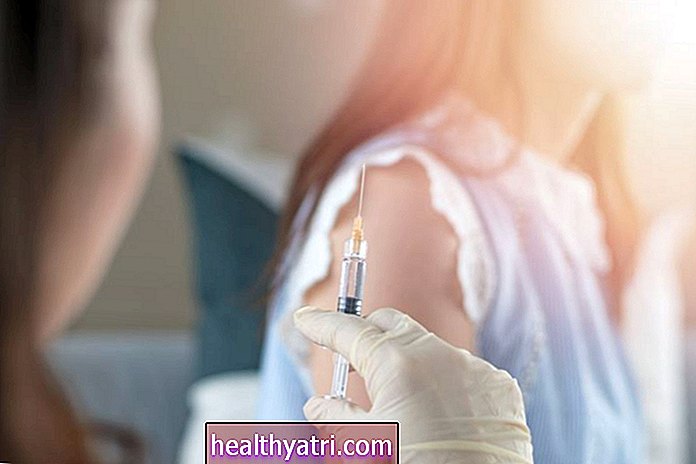
Pārtikas un zāļu pārvalde (FDA) 6. oktobrī paziņoja, ka tā prasīs, lai vakcīnu ražotāji COVID-19 koplietotu divus mēnešus ilgus drošības datus, pirms apstiprinās vakcīnu lietošanai plašākai sabiedrībai. FDA lēmums ir pieņemts. palielina sabiedrības neuzticību nākotnes COVID vakcīnas drošībai.
COVID-19 vakcīnas: sekojiet līdzi tam, kādas vakcīnas ir pieejamas, kas tās var saņemt un cik drošas tās ir.
FDA jaunās prasības
Saskaņā ar FDA jaunajām prasībām būs nepieciešami divu mēnešu pēcpārbaudes dati par klīnisko pētījumu brīvprātīgo veselību pēc tam, kad viņi būs saņēmuši otrās vakcīnas devas. FDA var izvēlēties piešķirt vakcīnu ražotājam ārkārtas lietošanas atļauju. - apzīmējums, kas ļauj produktu izmantot sabiedrībai, ja tiek izpildītas jaunās prasības.
Shobha Swaminathan, MD
Drošība ir ļoti svarīga, lai pārliecinātos, ka cilvēki uzticas mūsu paveiktajam darbam.
- Shobha Swaminathan, MDFDA savās vadlīnijās paskaidroja, ka vēlas redzēt datus no 3. fāzes pētījumiem, kad dalībnieki ir pabeiguši pilnu vakcīnas režīmu un divus mēnešus pēc tam. FDA uzskata, ka šī grafika sniegs "atbilstošu informāciju, lai novērtētu vakcīnas ieguvuma un riska profilu".
Saskaņā ar pamatnostādnēm FDA aplūkos "nevēlamus notikumus, smagas COVID-19 slimības gadījumus starp pētāmiem subjektiem un COVID-19 gadījumus, kas rodas laika posmā, kad vakcīnai ir adaptīvas (nevis iedzimtas) un atmiņas imūnās atbildes. būtu atbildīgs par aizsargājošu efektu. "
FDA arī saka, ka pētāmo personu vidū ir jābūt “pietiekamiem smagas pakāpes COVID-19 gadījumiem”, lai pierādītu, ka ir mazs risks, ka cilvēkiem var rasties nopietnas vakcīnas komplikācijas.
Turklāt FDA sagaida, ka ražotāji pierāda datus, kas saistīti ar noteiktiem sindromiem, konkrēti, ar vakcīnu saistītu pastiprinātu elpošanas ceļu slimību (ERD) no vakcīnas. “Kopumā pieci vai vairāk smagi COVID-19 gadījumi placebo grupā būtu pietiek, lai novērtētu, vai smagais COVID-19 gadījumu sadalījums starp vakcīnu un placebo grupām atbalsta labvēlīgu ieguvumu un riska profilu vai gluži pretēji rada bažas. "
Pašlaik klīnisko pētījumu 3. fāzē (pēdējā fāzē) ir 11 vakcīnas. Tomēr vairāki pētījumi, ko veica vairāki lieli farmācijas uzņēmumi, nesen ir apturēti pēc tam, kad vismaz vienam pētījuma dalībniekam ir izveidojusies nopietna, neizskaidrojama slimība.
Lieta gaidīt 2 mēnešus
"Es domāju, ka ir lieliski, ka FDA pieprasa, lai mums būtu divu mēnešu drošības dati," infekcijas slimību eksperts Shobha Swaminathan, MD, asociētais profesors un galvenais pētnieks Moderna COVID-19 vakcīnas izmēģinājumā Rutgers New Jersey Medical School Klīnisko pētījumu centrs, stāsta Verywell. "Drošība ir ļoti svarīga, lai pārliecinātos, ka cilvēki uzticas mūsu paveiktajam darbam."
Svaminatans skaidro, ka visbiežāk vakcīnu izraisītās blakusparādības rodas divu mēnešu laikā. “Lielākā daļa vakcīnas blakusparādību, piemēram, drudzis, nogurums un reakcijas injekcijas vietā, rodas pirmās nedēļas laikā, un sarežģītākas var rasties sešu nedēļu laikā. Tāpēc vismaz divi mēneši ir noderīgi, lai noteiktu, kas var notikt. ”
Shobha Swaminathan, MD
Nevajag izdarīt secinājumus par zinātnisko procesu. Tur ir daudz dezinformācijas.
- Shobha Swaminathan, MDSvaminatans saka, ka laika grafiks "cenšas sabalansēt sabiedrības vajadzības, neapdraudot drošību". Viņa cer, ka FDA norādījumi palīdzēs mainīt sabiedrības priekšstatu par vakcīnu izstrādes procesu.
"Sabiedrībā valda uzskats, ka COVID-19 vakcīnas pētījumi tiek virzīti ātrāk par grafiku, un daži cilvēki ir noraizējušies, ka tas nāk par drošības pasākumu cenu, kas patiesībā nav taisnība," saka Svaminatans. "FDA. pieņems lēmumu, vai viņu rīcībā esošā [pētnieku] informācija par drošību ir pietiekama. ”
Kopumā Svaminatans mudina cilvēkus uzticēties procesam. "Nevajag izdarīt secinājumus par zinātnisko procesu. Tur ir daudz dezinformācijas. ”
Ko tas jums nozīmē
FDA prasībai pēc divu mēnešu pēcpārbaudes datiem pēc tam, kad cilvēki saņem COVID-19 vakcīnu, vajadzētu palīdzēt nodrošināt, ka visas potenciālās blakusparādības tiek noķertas, pirms vakcīna ir pieejama plašai sabiedrībai. Tomēr galu galā process var aizņemt vairāk laika.
Sabiedrībai vajadzētu uzticēties tam, ka vakcīnas izstrādes un apstiprināšanas process ir drošs un ka FDA neapstiprinās vakcīnu, kamēr tā nebūs gatava un droša.






-to-treat-bedwetting-children.jpg)



-is-diagnosed.jpg)