Melflufēns (melfalāna flufenamīds) ir jauna zāle, kas tiek pētīta recidivējošas vai refraktāras multiplās mielomas (RRMM) ārstēšanā. Tas ir ķīmijterapijas zāļu melfalāna atvasinājums. Melflufēns ir peptīdu un zāļu konjugāts; melfalāna un peptīda (maza proteīna) kombinācija, kas savienota kopā. Melflufēnu ievada intravenozas infūzijas veidā (vēnā).
Zāles kā jaunu zāļu pieteikumu tika iesniegtas ASV Pārtikas un zāļu pārvaldē (FDA) 2020. gada jūlijā. FDA piešķīra pieteikuma prioritātes pārskatīšanu, un lēmums ir gaidāms 2021. gada februāra beigās. Melflufēns vēl nav plaši pieejams, jo tas nav licencēts un apstiprināts lietošanai mielomas gadījumā. Tomēr pacienti var tikt ārstēti ar zālēm kā daļa no klīniskā pētījuma.
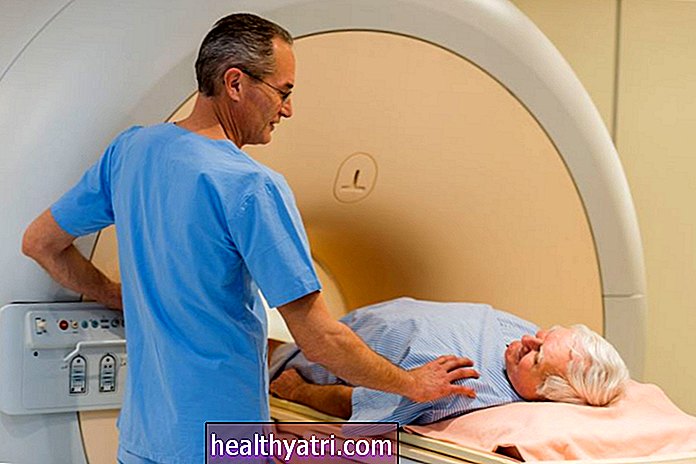
SimpleImages / Getty Images
Kas ir multiplā mieloma?
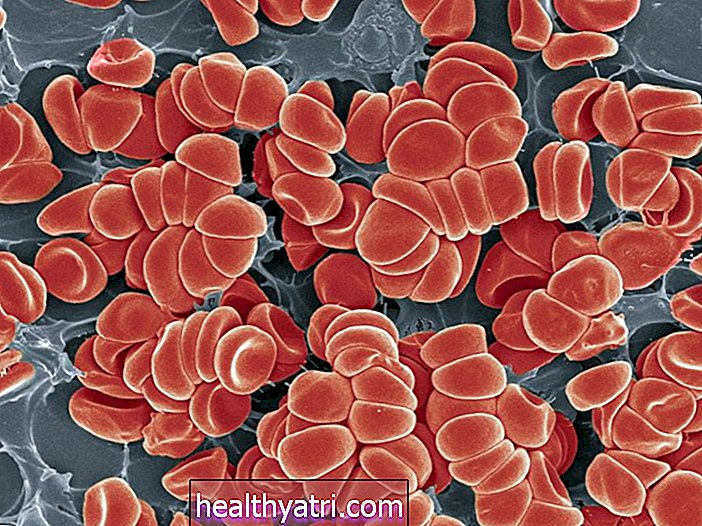
Multiplā mieloma ir reta, neārstējama asins vēža veids, ko sauc arī par hematoloģisko vēzi. Tas ietekmē šūnas, ko sauc par plazmas šūnām, kas ir balto asins šūnu veidi. No multiplās mielomas nav iespējams izārstēt, un tā gandrīz vienmēr atgriežas, un tajā brīdī jums tiek teikts, ka jums ir “recidivējoša vai refraktāra” slimība.
Kā darbojas Melflufen?
Tā kā agrākās terapijas līnijās tiek ieviestas jaunas pret mielomas zāļu kombinācijas, cilvēkiem ar RRMM bieži ir slimība, kas ir izturīga pret vairākām zālēm, tāpēc steidzami nepieciešamas zāles ar jauniem darbības mehānismiem.
Melflufēns, kombinācijā ar steroīdu deksametazonu, var aizpildīt šo neapmierināto medicīnisko vajadzību, nodrošinot:
- Jauns darbības mehānisms
- Klīniski nozīmīga efektivitāte
- Pārvaldāma drošība
Melflufēns iznīcina mielomas šūnas, izmantojot peptidāzes (fermentus, kas noārda peptīdus), kas mielomas šūnās bieži sastopami vairāk nekā veselās šūnās. Kad melflufēns nonāk mielomas šūnās, šūnā esošās peptidāzes pārtrauc saiti, kas tur melfalāns un peptidāze kopā. Tas atbrīvo aktīvo melfalānu mielomas šūnā. Tad melfalāns izraisa neatgriezeniskus DNS bojājumus, kas izraisa šūnu nāvi.
Ko saka pētījums
Tiek turpināti pētījumi, lai atrastu jaunas multiplās mielomas ārstēšanas metodes un izstrādātu veidus, kā uzlabot esošo ārstēšanu.
Lai palīdzētu veikt pētījumus, ārstēšanas laikā jums var lūgt piedalīties klīniskajā pētījumā.
Pašlaik Melflufen tiek pētīts kā ārstēšana RRMM pacientiem klīnisko pētījumu apstākļos. Klīniskie pētījumi, kuros pētīta melflufēna efektivitāte, ietver:
O-12-M1 pētījums
O-12-M1 bija starptautisks, daudzcentru I / II fāzes pētījums, lai noteiktu melflufēna devu kombinācijā ar deksametazonu un izpētītu ārstēšanas reakciju pacientiem ar RRMM, kuri bija izturīgi (izturīgi) pret pēdējo terapijas līniju. A
O-12-M1 pētījumā 45 pacientu grupa, kas bija saņēmusi vismaz divas iepriekšējas terapijas, tika reģistrēta laikā no 2013. gada jūlija līdz 2016. gada decembrim. Pētījumā tika mēģināts atklāt maksimāli pieļaujamo melflufēna devu. Noteiktā maksimālā pieļaujamā deva bija 40 mg melflufēna kombinācijā ar deksametazonu.
Pārbaudītā lielākā kohorta grupa (55 mg) pārsniedza maksimāli pieļaujamo devu, jo četriem no sešiem pacientiem bija smagas blakusparādības, tostarp neitropēnija (zems leikocītu līmenis) un trombocitopēnija (zems trombocītu skaits); tāpēc plānotā lielākā 70 mg deva netika pārbaudīta.
Pētījuma pacientiem ārstēšana ar melflufēnu un deksametazonu izraisīja slimības stabilizēšanos 76% pacientu.
Vidējais laiks līdz nākamajai terapijai - terapijas sākumam līdz nākamajai terapijai (vai pacienta nāvei, atkarībā no tā, kas notika agrāk) - bija 7,9 mēneši. Pacienti dzīvoja vidēji 20,7 mēnešus.
HORIZON klīniskais pētījums
II fāzes HORIZON klīniskajā pētījumā, kas notika 20 vietās visā ASV un Eiropā, melflufēnu un deksametazonu saņēma 154 pacienti, kuri bija saņēmuši vidēji piecas iepriekšējās ārstēšanas līnijas.
Visi pacienti iepriekš tika ārstēti ar imūnmodulējošām zālēm un proteasomu inhibitoriem, un viņi bija izturīgi pret pomalidomīdu un / vai daratumumabu.
Aptuveni trīs no katriem 10 pacientiem (29%) reaģēja uz ārstēšanu, un vidējais laiks pirms mielomas atkārtošanās bija četri mēneši. Šie rezultāti parādīja, ka melflufēns var būt noderīgs pacientiem, kuriem iepriekš ir bijušas vairākas ārstēšanas līnijas.
Nevēlamās blakusparādības (AE) izraisīja melflufēna devas samazināšanu 27% pacientu un devas aizkavēšanos 61% pacientu. Visizplatītākā AE, kas izraisīja devas samazināšanu, bija trombocitopēnija (zems trombocītu skaits), kas novēroja 14% pacientu.
Nopietnas AE radās 49% pacientu kopumā; visbiežāk ziņots par pneimoniju (9%) un neitropēniju (5%). Otrais primārais ļaundabīgais audzējs notika pieciem pacientiem; no tiem četriem bija ļaundabīgi audzēji ar ādas izpausmēm. Kopumā 10 pacienti (6%) nomira no ar ārstēšanu saistīto blakusparādību dēļ.
Devas
Melflufēnu ievada intravenozas infūzijas veidā (vēnā). Klīniskajos pētījumos deva ir bijusi:
- 40 mg melflufēna katra ārstēšanas cikla pirmajā dienā
40 mg deksametazona (samazināta deva pacientiem no 75 gadu vecuma) katra 28 dienu cikla 1., 8., 15. un 22. dienā
Dažos pētījumos deva tika samazināta tiem, kuriem bija nevēlama reakcija.
Blakus efekti
Visbiežāk novērotās melflufēna blakusparādības ir:
• Zems asins šūnu skaits - neitropēnija un trombocitopēnija
• anēmija
• Nogurums
• Infekcijas, ieskaitot pneimoniju un augšējo elpceļu infekcijas
• Slikta dūša un caureja
Tā kā melflufēns ir salīdzinoši jauna zāle, var parādīties jaunas blakusparādības, par kurām vēl nav ziņots.
Riski
Tā kā pētījumi turpinās, ir grūti novērtēt riskus, kas saistīti ar melflufēna lietošanu RRMM. Tā kā pacienti, kas pieņemti darbā klīniskajos pētījumos, bieži vien ir izsmēluši iepriekšējo ārstēšanu, ir iespējama negatīva ietekme vai pat nāve ārstēšanas laikā un pēc tās.
Infekcijas ir galvenais saslimstības un mirstības cēlonis pacientiem ar RRMM sakarā ar novājinātu imūnsistēmu. Ir svarīgi regulāri novērot, vai Jums nav infekcijas pazīmju, un cik drīz vien iespējams ziņot ārstam par visām bažām.