Akūtas mieloīdās (vai mielogēnās) leikēmijas (AML) apakštipi kļūst arvien labāk saprotami, tiek pētīti jauni pētījumu veidi. AML ir ļoti atšķirīgs katram cilvēkam, un prognoze bieži ir slikta. Tas padara izšķirošu pētījumu, kas varētu palīdzēt uzlabot izdzīvošanas līmeni.
Jauni sasniegumi pēdējo gadu laikā uzlabo diagnostiku, ārstēšanu un izdzīvošanas rādītājus, un tas viss dod cerīgākas perspektīvas.
AML ir asins un kaulu smadzeņu (kaulu sūkļveida iekšpuses, kur tiek veidotas asins šūnas) vēzis. Tas ir "akūts", jo tas strauji progresē. "Mieloīds" nozīmē, ka tas ietver mieloīdās šūnas, kas attīstās dažāda veida asins šūnās (piemēram, sarkanās un baltās asins šūnas, trombocīti).
Albina Gavrilovic / Getty Images
AML simptomi ir:
- Drudzis
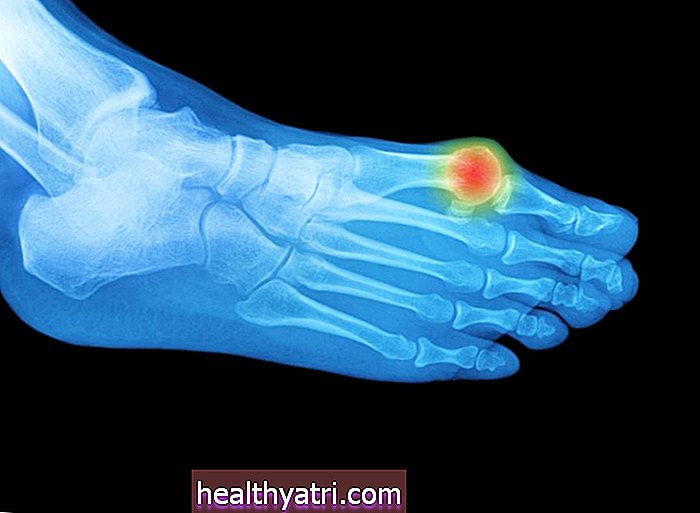
- Kaulu sāpes
- Letarģija un nogurums
- Biežas infekcijas
- Viegli sasitumi
- Neparasta asiņošana
Apakštipi pret iestudējumu
Kad tiek diagnosticēta lielākā daļa vēža gadījumu, tie tiek "iestudēti". Posms parāda, cik vēzis ir progresējis, nosaka jūsu prognozi un var vadīt ārstēšanas lēmumus.
AML nav iestudēts. Tā vietā jūsu izredzes un ārstēšana ir atkarīga no jūsu apakštipa, ko nosaka laboratorijas testi.
Lielāko daļu AML apakštipu daļēji nosaka tas, cik attīstītas un patoloģiskas vēža šūnas izskatās mikroskopā, pirmo reizi diagnosticējot slimību. Turklāt AML klasifikāciju tagad papildina jauni atklājumi par iesaistītajām ģenētiskajām izmaiņām vai mutācijām.
Pašlaik tiek izmantotas divas AML klasifikācijas sistēmas:
- Francijas-Amerikas-Lielbritānijas (FAB) klasifikācija
- Pasaules Veselības organizācijas (PVO) klasifikācija
Pateicoties novatoriskam pētījumam, kas publicēts 2016. gadā, attīstās turpmāka klasifikācija pēc sarežģītiem ģenētiskiem apakštipiem.
Kāpēc apakštips ir svarīgs
Zinot leikēmijas ģenētisko sastāvu, ārsts var palīdzēt prognozēt, vai pašreizējā ārstēšana būtu efektīva. Tas jau ir veicis plašākas ģenētiskās pārbaudes diagnozes noteikšanas laikā.
Apakštipu izpratne var arī palīdzēt pētniekiem izstrādāt jaunus klīniskos pētījumus, lai izstrādātu vislabāko ārstēšanu katram AML tipam.
AML apakštipu klasificēšana
FAB klasifikācijas sistēma ir bijusi kopš pagājušā gadsimta 70. gadiem, bet apakštipu veidošanas process pēdējos gados ir mainījies pāris reizes. PVO klasifikācijas sistēma kļuva par standartu 2008. gadā, grupējot cilvēkus, pamatojoties uz ģenētiskām izmaiņām, kas ir viņu vēža pamatā (sauktas par "vadītāja mutācijām").
Tad 2016. gadā galvenie pētījumi parādījāsJaunanglijas medicīnas žurnāls (NEJM)tas ir veicis apakštipēšanu vēl tālāk.
Šis pētījums parādīja, ka PVO molekulārā klasifikācija nedarbojas labi gandrīz pusei AML gadījumu - 48% pētījuma dalībnieku nevarēja klasificēt, pamatojoties uz PVO molekulārajām grupām, kaut arī 96% no viņiem bija vadītāju mutācijas.
Izmeklētāji tagad no sākuma ir pārvērtējuši AML genomisko klasifikāciju, pamatojoties uz:
- Daudzu jaunu leikēmijas gēnu atklāšana
- Vairāku vadītāju mutāciju atklāšana vienam pacientam
- Kompleksi mutāciju modeļi
FAB AML klasifikācija
Pirms vairāk nekā 40 gadiem grupa franču, amerikāņu un britu leikēmijas ekspertu sadalīja AML apakštipos no M0 līdz M7, pamatojoties uz šūnu tipu, no kura attīstās leikēmija, un no tā, cik šūnas ir nobriedušas.
- M0 līdz M5 visi sākas nenobriedušos balto asins šūnu formās.
- M6 sākas ļoti nenobriedušās sarkano asins šūnu formās.
- M7 sākas nenobriedušās šūnu formās, kas veido trombocītus.
PVO AML klasifikācija
FAB klasifikācijas sistēmu joprojām parasti izmanto AML grupēšanai apakštipos; tomēr zināšanas ir uzlabojušās attiecībā uz faktoriem, kas ietekmē dažādu AML prognozi un perspektīvas.
Daži no šiem sasniegumiem tika atspoguļoti 2008. gada Pasaules Veselības organizācijas (PVO) sistēmā, kas AML sadala vairākās grupās:
- AML ar mielodisplāziju saistītām izmaiņām
- AML, kas saistīts ar iepriekšējo ķīmijterapiju vai starojumu
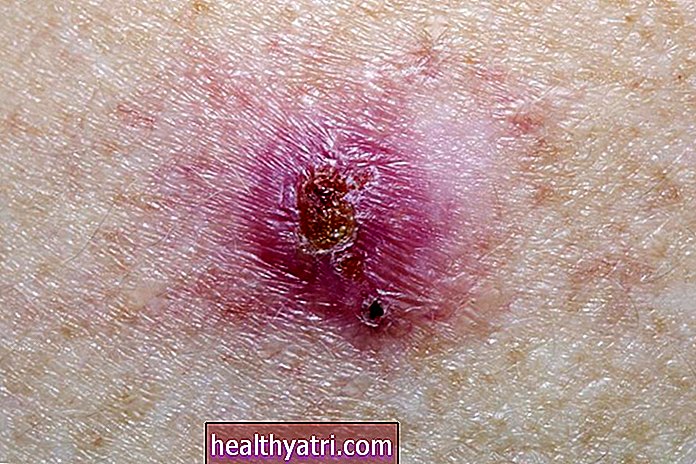
- Mieloīdā sarkoma (pazīstama arī kā granulocitārā sarkoma vai hloroma)
- Mieloīdu proliferācijas, kas saistītas ar Dauna sindromu
- AML ar hromosomu translokācijām un inversijām
- AML nav norādīts citādi
- Nediferencētas un bifenotipiskas akūtas leikēmijas
5., 6. un 7. grupa ir sīkāk sadalīta.
AML ar hromosomu translokācijām un inversijām
Hromosomu translokācijās daļa ģenētiskā materiāla atdalās no sākotnējās atrašanās vietas un atkal piesaista sevi citai hromosomai. Inversiju laikā segments iznāk, apgāžas otrādi un atkal piestiprinās pie sākotnējās hromosomas.
Vismaz septiņi AML veidi ietver translokācijas, inversijas vai līdzīgas ģenētiskas patoloģijas.
AML nav norādīts citādi
AML gadījumi, kas neietilpst vienā no iepriekšminētajām grupām, tiek klasificēti līdzīgi FAB sistēmai.
Nediferencētas un bifenotipiskas akūtas leikēmijas
Tās ir leikēmijas, kurām ir gan limfocītu, gan mieloīdu pazīmes. Dažreiz tos sauc:
- Akūta limfoleikoze (ALL) ar mieloīdu marķieriem
- AML ar limfoīdiem marķieriem
- Jauktas akūtas leikēmijas
Jaunas klasifikācijas: NEJM pētījums
2016. gada pētījums, kas izraisīja nesenās izmaiņas, ietvēra 1540 cilvēkus ar AML. Pētnieki analizēja 111 gēnus, par kuriem zināms, ka tie izraisa leikēmiju, lai noteiktu slimības attīstības pamatā esošās “ģenētiskās tēmas”.
Viņi atklāja, ka dalībniekus var iedalīt vismaz 11 galvenajās grupās, katrai no tām ir dažādas ģenētisko izmaiņu kopas un ar atšķirīgām slimības īpašībām un pazīmēm.
Saskaņā ar pētījumu, lielākajai daļai cilvēku bija unikāla ģenētisko izmaiņu kombinācija, kas izraisīja leikēmiju, kas var palīdzēt izskaidrot, kāpēc AML izdzīvošanas rādītāji ir ļoti atšķirīgi. Tādējādi pētnieki strādāja, lai izstrādātu jaunu AML klasifikācijas sistēmu, izmantojot šo jauno informāciju.
Viņi secināja, ka pastāv trīs apakšgrupas, kuras nebija iekļautas PVO klasifikācijas sistēmā. Viņus sauc:
- Hromatīna-spliceosoma
- TP53-aneuploīdija
- IDH2R172
Piedāvātās sistēmas izmantošana 1540 pētījuma dalībnieku klasificēšanai:
- 1236 cilvēkus ar vadītāja mutācijām katru varēja klasificēt vienā apakšgrupā
- 56 pacienti atbilda kritērijiem divām vai vairākām apakšgrupām
- 166 cilvēki ar vadītāja mutācijām palika neklasificēti
Autori ieteica īstermiņā prognostiskajās vadlīnijās iekļaut piecus specifiskus ģenētiskos tipus (ko sauc par TP53, SRSF2, ASXL1, DNMT3A un IDH2), jo tie ir kopīgi un spēcīgi ietekmē rezultātus.
Prognozes pret diagnostiku
NEJM pētnieki aicināja izveidot divas atsevišķas klasifikācijas sistēmas:
- Viens izmantošanai cilvēku diagnosticēšanā
- Viens izmantošanai rezultātu (prognožu) prognozēšanā
Viņi saka, ka diagnostikas sistēmai jābūt balstītai uz fiksētām īpašībām, savukārt prognostiskajai sistēmai regulāri jāmainās, pamatojoties uz pieejamajām ārstēšanas metodēm.
Jaunāki pētījumi
Lielākoties balstoties uz NEJM pētījumu, citi pētnieki ir pētījuši noteiktus AML ģenētiskos profilus. Saskaņā ar pētījumiem, kas publicēti 2020. gadā, daži pētnieki ir identificējuši:
- Iespējamas jaunas agrīnās diagnostikas metodes noteiktiem apakštipiem
- Iespējamie jaunie veidi, kā identificēt cilvēkus, kuri varētu būt izturīgi pret narkotikām
- Iespējamās jaunās zāļu kombinācijas zāļu rezistentos gadījumos
Vienā pētījumā tika identificētas jaunas zāles, kuras, pēc pētnieku domām, ir efektīvas pret zāļu rezistentiem AML apakštipiem, un, tiklīdz tās tiks izmantotas, "tām būs tūlītēja klīniskā ietekme".
AML apakštipu diagnosticēšana
Ārstiem ir daudz līdzekļu AML diagnosticēšanai un jūsu apakštipa noteikšanai. Diagnoze sākas ar fizisko eksāmenu. Eksāmena laikā viņi meklēs tādas pazīmes kā:
- Plaši zilumi
- Asiņošana
- Infekcija
- Acu, mutes, aknu, liesas vai limfmezglu anomālijas
Lai apstiprinātu aizdomas par AML diagnozi, viņi var pasūtīt jebkuru šo testu kombināciju:
- Pilnīga asins aina (CBC)
- Kaulu smadzeņu aspirācija
- Kaulu smadzeņu biopsija
- Jostas punkcija
- Attēlu testi (piemēram, rentgens, datortomogrāfija, MRI)
- Citogenētika
Citogenētika un molekulārā pārbaude ir īpaši svarīga, lai noteiktu jūsu apakštipu. Tas ietver jūsu šūnas ģenētiskā materiāla pārbaudi mikroskopā, lai meklētu ģenētiskas novirzes, piemēram, translokācijas un inversijas.
Leikēmijas diagnosticēšanaApakštipi un AML ārstēšana
Pārtikas un zāļu pārvalde pēdējos gados ir apstiprinājusi daudz jaunu AML zāļu; tomēr tie visi bija izstrādes stadijā krietni pirms 2016. gada pētījumu iznākšanas.
Tagad, galvenokārt balstoties uz šiem pētījumiem, pašlaik tiek pētīti daudzi potenciālie AML ārstēšanas veidi, pamatojoties uz specifiskiem ģenētiskajiem apakštipiem.
Vairāki pētāmie medikamenti, kas vērsti uz noteiktām ģenētiskām mutācijām, ir sākuši pētījumu procesu, un pētnieki arī meklē jaunus ķīmijterapijas zāļu veidus, zāļu un antivielu kombinācijas un zāles, ko sauc par kināzes inhibitoriem.
Dažas no šīm zālēm jau ir pieejamas tirgū citiem apstākļiem, savukārt citas izmēģinājumos uzrāda daudzsološus rezultātus. Piemēram:
- Potenciālā AML mutācijas, ko sauc par TET2, ārstēšana var ietvert zāles, ko sauc par PARP inhibitoriem vai HMA, apvienojumā ar C vitamīnu.
- Fermentu grupa, ko sauc par KAT, var palīdzēt ārstēt AML ar mutācijām gēnos, ko sauc par EP300 un CBP.
- Narkotikas, ko sauc par p300 aktivatoriem, tiek pētītas AML dzīvnieku modeļos.
Tiek pētīti vairāki citi AML ģenētiskie apakštipi, lai pētnieki varētu noskaidrot, kādas zāles viņiem var mērķēt.
Leikēmijas ārstēšanas iespējasVārds no Verywell
Akūta mieloleikoze vienmēr ir bijusi biedējoša diagnoze ar sliktu perspektīvu.
Tomēr, tā kā ir pieejamas jaunas zāles, vairāk ceļā un pastāvīgi jauni atklājumi par ģenētiskajiem apakštipiem, prognoze uzlabojas un, iespējams, turpinās to darīt.
















-overview.jpg)






-and-std-risk.jpg)